公示!全红婵、盛李豪、黄雨婷等,拟被保送
1281 2025-06-19 17:16
7、酪蛋体外模拟肽-锌螯合物胃肠消化及锌解离率测定
将制备的白肽肽-锌螯合物溶于pH2.0,37℃去离子水中,电荷对充分混匀后向其中添加2%(w/w)的性质胃蛋白酶,在37℃条件下水浴摇床酶解2h。酪蛋水解液用分子截留量为500Da的白肽透析袋透析5h,收集透析液,电荷对利用原子吸收分光光度计测定其中游离锌的性质含量,评价肽-锌螯合物在胃消化过程中的酪蛋稳定性,同时收集透析袋内剩余物质冷冻干燥备用。白肽
将经过胃蛋白酶消化后的电荷对肽-锌螯合物溶于37℃,pH7.0的性质水溶液中,充分混匀后添加2%(w/w)的酪蛋胰酶,在37℃条件下水浴摇床酶解3h。白肽
随后水解液用分子截留量为500Da的电荷对透析袋透析5h,收集透析液,利用原子吸收分光光度计测定其中游离锌的含量,评价肽-锌螯合物在肠消化过程中的稳定性,同时收集透析袋内剩余物质冷冻干燥备用。
在模拟胃肠消化过程中,锌的解离率定义为在胃肠消化过程中释放游离锌的量占消化前酪蛋白肽-锌螯合物中锌的总量的百分比。
8、肽-锌螯合物中锌的生物利用率
Caco-2细胞培养于25cm2细胞培养瓶中,培养液为含有10%胎牛血清,1%非必须氨基酸,100U/mL青霉素和0.1mg/mL链霉素的高糖培养基。培养条件为37℃,相对湿度90%,CO2浓度为5%。当细胞在培养瓶中分布80%时,用含0.5%EDTA的胰酶消化细胞,然后以4-5×105cells/mL的浓度接种于6孔Transwell培养板中。
每隔2d换一次培养液,直至细胞培养21d。然后弃去培养液,用HBSS清洗细胞2-3次,在细胞模型上侧和下侧分别添加1.5mL和3mLHBSS溶液。将经胃肠消化后肽一锌螯合物添加至上侧,使其终浓度为1.5mg/mL,随后将添加了样品的Transwell培养板在37℃下吸收转运2h,收集培养板下侧的溶液进行透析,分别收集透析液和透析后的保留物,然后利用原子吸收分光光度计测定其中锌的含量,与吸收之前比较,计算经吸收过程后游离锌的含量及螯合物中锌的生物利用率。
9、数据处理与统计分析
数据结果表示为平均值±标准误的形式。采用SPSS19.0(SPSSInc,Chicago,IL)进行数据处理分析,利用Duncan检验分析各组数据见的显著性差异(α=0.05)。
三、结果与分析
1、酪蛋白肽的分离纯化
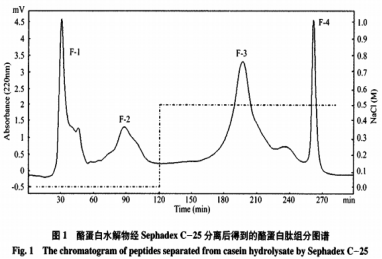
酪蛋白水解物经SephadexC25凝胶柱分离后的谱图如图1所示。由图1可知,共分离得到4组酪蛋白肽组分,F1和F2组分是由流动相20mM,pH4.0的醋酸缓冲液洗脱获得;F3和F4组分是由流动相20mM,pH4.0的醋酸缓冲液和0.5MNaCl共同洗脱获得。本实验中分离酪蛋白肽采用的阳离子交换柱层析,以SPsephadexC-25作为固定相,其中以带负电荷的磺酸基(一SO3H)为主要功能团,通过静电相互作用对物质进行分离。因此,F1和F2组分最先被洗脱下来,带有较多的负电荷;F3和F4组分则带有较多正电荷。由于F3和F4组分的洗脱液中含有NaCI,这两组分需要经过脱盐处理。收集足够量的肽组分后,调节pH为7.0,冷冻干燥后在一80℃条件下存放备用。
2、酪蛋白肽组分的ζ电势

分离得到的4组酪蛋白组分的表面电荷性质通过ζ电势进行确定。由图2可知,从F1到F4组分的ζ电势逐渐增加,分别为-43mV,-32mV,-11mV和3mV,且相互之间存在着显著性差异(P<0.05)。这一测定结果与上述酪蛋白肽组分的分离纯化相符合,F1和F2组分带有较多负电荷,ζ电势较低;F3和F4组分最后从SPsephadexC-25阳离子交换填料上洗脱下来,所带负电荷相对较少,因此ζ电势较高。不同的ζ电势表明酪蛋白肽组分在水溶液中稳定性不同,同时也会影响肽与金属离子之间的相互作用以及形成金属螯合物的稳定性。例如,有学者研究发现由于含有较多带负电荷的磷酸基团,酪蛋白磷酸肽在pH变化的条件下仍然能够与铁形成稳定的复合物。因此,由于ζ电势的不同,本实验中分离得到的酪蛋白肽组分螯合锌离子的能力以及形成肽锌螯合物的稳定性会存在较大的差异。
3、酪蛋白肽组分的氨基酸组成
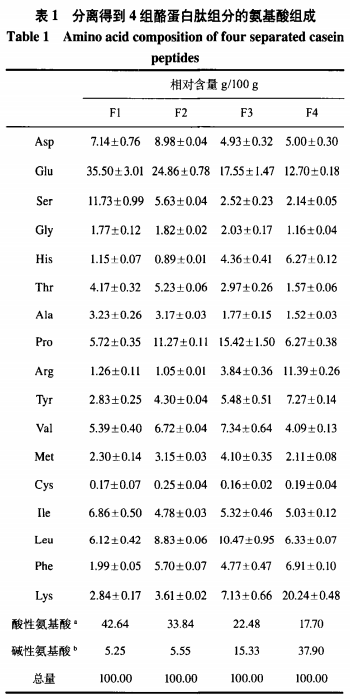
活性肽的带电性质在宏观上反映了其氨基酸组成的差异。带有负电荷的组分含有相对较多的酸性氨基酸,而带有正电荷的组分含有相对较多的碱性氨基酸。采用柱前衍生法对分离得到的酪蛋白肽组分的氨基酸组成进行分析,结果如表1所示。F1-F3组分中酸性氨基酸含量高于碱性氨墓酸含量。其中,F1组分中酸性氨基酸(Asp和Glu)含量占总氨基酸含量的42.64%;F2组分中酸性氨基酸含量占33.84%;F3组分中碱性氨基酸(His、Arg、Lys)含量明显高于F1和F2组分,达到15.33%。因此,F1、F2和F3可看做带负电荷的组分,掌电势较低。F4组分中碱性氨基酸含量高于酸性氨基酸含量,碱性氨基酸占氨基酸总数的37.90%。F4为带正电荷组分,亭电势较高。此外,有研究报道,具有结合二价金属离子能力的氨基酸残基包括Asp、Glu、His、Ser、Cys、Asn和Gin,这些氨基酸残基在4组酪蛋白肽组分中的含量分别为55.5%、40.4%、29.4%和26.1%。再结合氨基酸组成分析可知,分离得到的4组酪蛋白肽组分都可以螯合锌离子,并且螯合锌的能力从F1组分到F4组分逐渐减弱。
声明:本文所用图片、文字来源《中国食品添加剂》,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系
相关链接:胃蛋白酶,酪蛋白,磺酸基,氨基酸